la gran cantidad de compuestos orgánicos que existen tiene su explicación, en las características del átomo de carbono, que tiene cuatro electrones en su capa de valencia. según la regla del octeto necesita ocho para completarla, por lo que la forma enlaces con otros átomos.
el carbono forma también enlaces covalentes con facilidad para alcanzar una configuración estable, estos enlaces los forma con facilidad con otros carbonos lo que permite formar frecuentemente cadenas abiertas y cerradas.
QUE ES EL CARBONO
Es un elemento químico de numero 6 y símbolo C. como miembro del grupo de los carbonoideos de la tabla periódica de los elementos. es solido a temperatura ambiente dependiendo de las condiciones de formación, puede encontrarse en la naturaleza en distintas formas alotrópicas, carbono amorfo y cristalino en forma grafito o diamante respectivamente.

GRAFITO
Una de las formas en las cuales se encuentra el carbono es el grafito, que es el material del cual esta hecha la parte interior de los lapices de madera. El grafito tiene exactamente los mismos átomos del diamante, pero por estar dispuestos en diferente forma, su textura, fuerza y color son diferentes.

DIAMANTE
El diamante denota siete formas diferentes. Se aplica generalmente como recubrimientos a otros materiales que pueden beneficiarse de algunas de esas propiedades.
los siete contienen cantidades significativas de átomos de carbono hibridados en la forma sp3. la razón por la que hay diferentes tipos es que incluso en el diamante se puede encontrar en dos politipos cristalinas.
El habitual tiene sus átomos de carbono dispuestos en una red cubica, mientras que la muy frecuente forma alotropa posee una estructura hexagonal.

HULLA
Es una roca sedimentaria orgánica, un tipo de carbón mineral que contiene entre un 45 y un 85 por ciento de carbono. es dura y quebradiza,estratificada, de color negro y brillo mate o graso.Hay tres clases de hullas:

HIBRIDACION DEL CARBONO
En un reacomodamiento de electrones del mismo nivel de energía (orbital s) al orbital del mismo nivel de energía. los orbitales híbridos explican la forma en que se disponen los electrones en la formación de los enlaces, dentro de la teoría del enlace de valencia, compuesta por nitrógeno liquido que hace compartirlas con cualquier otro elemento químico ya sea un alcano o comburente.
el carbono tiene un numero atómico 6 y n° de masa 12; en su núcleo tiene 6 protones y 6 neutrones. y esta rodeado por 6 electrones distribuidos:
- 2 en el nivel 1s
- 2 en el nivel 2s
- 2 en el nivel 2s
CARACTERÍSTICAS DE LA HIBRIDACION DEL CARBONO
hibridacion sp3 (enlace simple c-c )
En seguida, se híbrida el orbital 2s con los 3 orbitales 2p para formar 4 nuevos orbitales híbridos que se orientan en el espacio formando entre ellos, ángulos de separación de 109.5°.
A cada uno de estos orbitales se les denomina sp3 por que tienen 25% de carácter s y un 75% de carácter p.
Esta nueva configuración se llama átomo de carbono híbrido y al proceso de transformación se llama hibridacion.
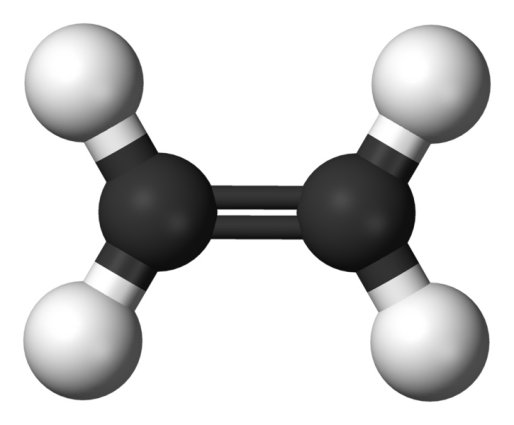
HIBRIDACION SP2 (ENLACE DOBLE C=C )
Los átomos de carbono también pueden formar entre si enlaces llamados insaturaciones dobles, en donde la hibridacion ocurre entre el orbital 2s y dos orbitales 2p quedando un orbital p sin hibridar, se producirán 3 orbitales sp2.
HIBRIDACION SP (ENLACE TRIPLE)
Se define como la combinación de un orbital s y un p, para formar 2 orbitales híbridos, con orientación lineal. Este es el tipo de enlace híbrido, con un angulo de 180° y que se encuentra existente en compuestos con triples enlaces como los alquinos.
IMAGEN DEL SP3

IMAGEN DEL SP

IMAGEN DEL SP2
muy bien
ResponderEliminarMuchas gracias. Me ayudó mucho.♥
ResponderEliminarOkay
ResponderEliminarcuales son los tipos dímelos porfa de hibridacion
ResponderEliminarLos tipos ahí están son los sp sp2 y sp3
Eliminar